京津冀联合出台机构备案后首次检查和日常检查标准的意见稿

为进一步贯彻落实国家京津冀协同发展战略,构建促进药物临床试验监管领域协同发展的标准体系及制度保障,加强药物临床试验机构监督管理,提升药物临床试验质量管理水平,服务医药产业高质量发展,依据《中华人民共和国药品管理法》《中华人民共和国疫苗管理法》《药品注册管理办法》《药物临床试验机构管理规定》《药物临床试验质量管理规范》等法规、规章及规范性文件,结合京津冀三地实际,北京市药品监督管理局会同天津市药品监督管理局、河北省药品监督管理局共同制定了《京津冀药物临床试验机构备案后首次监督检查标准(征求意见稿)》《京津冀药物临床试验机构日常监督检查标准(征求意见稿)》,现向社会公开征求意见,欢迎社会各界提出意见建议。
公开征集意见时间为:2021年2月24日至3月9日。
意见反馈渠道如下:
1.电子邮件:邮件主题请注明“备案后首次检查标准反馈意见”或“日常监督检查标准反馈意见”,邮箱地址:zhucechu@yjj.beijing.gov.cn
2.邮寄通信地址:北京市西城区枣林前街70号中环广场A座1313室药品注册管理处,邮政编码:100053。(请在信封上注明“意见征集”字样)
3. 传真:010-83560723
4. 电话:010-83979470
5. 登录北京市人民政府网站(http://www.beijing.gov.cn),在“政民互动”版块下的“意见征集”专栏中提出意见。
附件:
1.《京津冀药物临床试验机构备案后首次监督检查标准 (征求意见稿)》
2.《京津冀药物临床试验机构备案后首次监督检查标准 (征求意见稿)》起草说明
3.《京津冀药物临床试验机构日常监督检查标准(征求意见稿)》
4.《京津冀药物临床试验机构日常监督检查标准(征求意见稿)》起草说明
5.《征求意见反馈表》
北京市药品监督管理局
2021年2月24日
附件1
京津冀药物临床试验机构备案后首次监督检查标准(征求意见稿)
一、为规范京津冀药物临床试验机构备案管理,根据《中华人民共和国药品管理法》《中华人民共和国疫苗管理法》《药品注册管理办法》《药物临床试验机构管理规定》《药物临床试验质量管理规范》等法律法规及规范性文件,制定本检查标准。
二、本检查标准适用于京津冀行政区域内新备案药物临床试验机构、增加临床试验专业、地址变更备案后的首次监督检查。
三、检查标准分为机构、伦理委员会、专业、Ⅰ期临床试验研究室四个部分,包括19个检查环节、66个检查项目。其中关键项目13项(标示为“★”),一般项目53项。
四、检查中发现不符合要求的项目统称为“缺陷项目”。其中,关键项目不符合要求者称为“严重缺陷”,一般项目不符合要求者称为“一般缺陷”。
五、检查结果评定
检查结果按机构、伦理委员会、专业、Ⅰ期临床试验研究室四部分分别评定。
(一)各检查部分均未发现严重缺陷,且一般缺陷≤20%,判定为通过首次备案检查。要求机构对发现的问题应立即组织整改,并于10个工作日内将整改情况报告报送所在地药品监管部门,整改期间机构可继续承接药物临床试验。
(二)发现严重缺陷,或一般缺陷>20%的,判定为未通过首次备案检查,对发现的问题应立即组织整改。涉及机构或伦理委员会未通过备案检查的,整改期间该机构不得开展新的药物临床试验项目;涉及专业、Ⅰ期临床试验研究室未通过备案检查的,整改期间相关专业、Ⅰ期临床试验研究室不得开展新的药物临床试验项目。整改完毕后应向所在地药品监管部门提交整改报告及跟踪检查申请,现场检查符合要求后,方可开展新的药物临床试验。整改期间开展新的药物临床试验的,由所在地省级药品监管部门提请国家药监局取消该机构或专业备案。涉及违法行为的,依法查处,并向所在地省级卫生健康主管部门通报。
A.药物临床试验组织管理机构检查项目


注:A.药物临床试验组织管理机构检查项目包括6个检查环节、20个检查项目,其中关键项目3项,一般项目17项。
B.伦理委员会检查项目
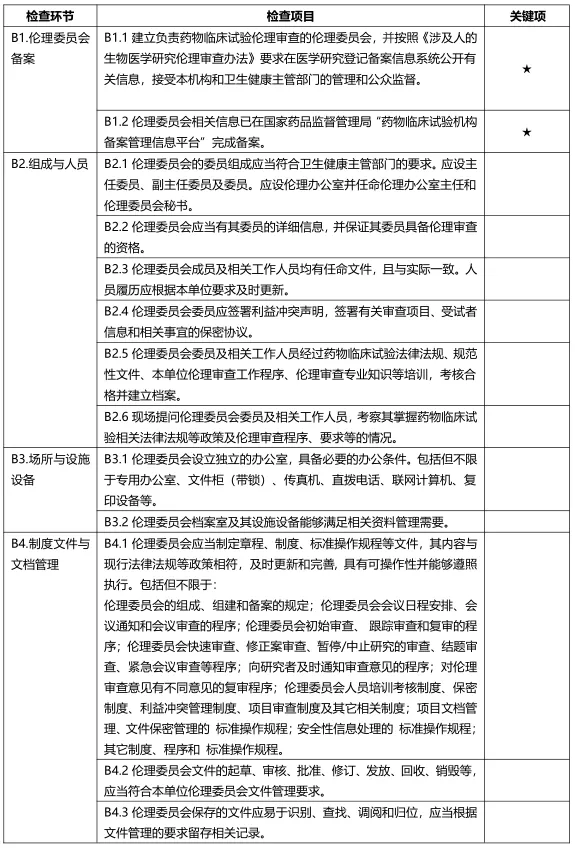
注:B.伦理委员会检查项目包括4个检查环节、13个检查项目,其中关键项目2项,一般项目11项。
C.专业检查项目


注:C.专业检查项目包括4个检查环节、17个检查项目,其中关键项目6项,一般项目11项。
D.Ⅰ期临床试验研究室专业检查项目
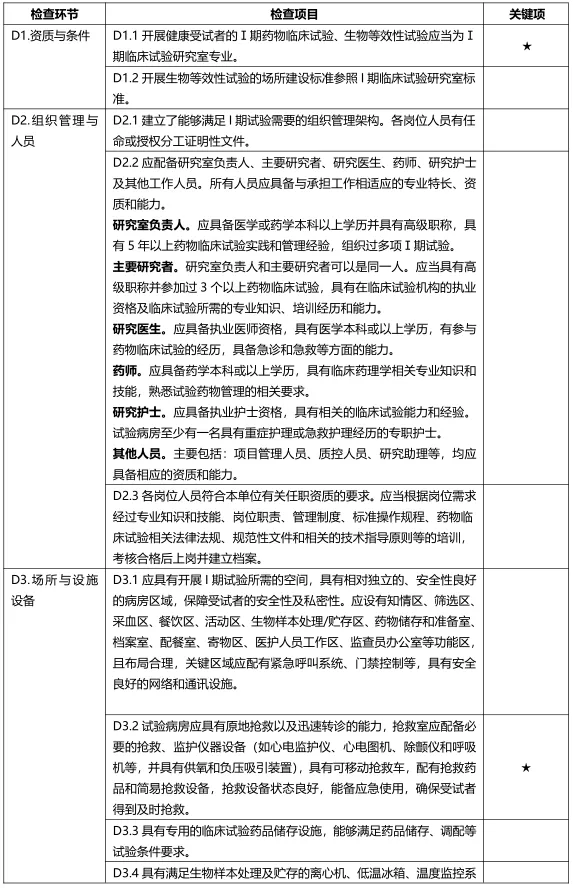

注:D.Ⅰ期临床试验研究室专业检查项目包括5个检查环节、16个检查项目,其中关键项目2项,一般项目14项。
附件2
《京津冀药物临床试验机构备案后首次监督
检查标准(征求意见稿)》起草说明
一、起草背景和必要性
药物临床试验是对药物安全性、有效性进行科学评价的一个重要环节,药物临床试验机构是试验运行及质量管理的责任主体,机构所具备的试验条件及临床试验质量管理体系直接关系到试验数据的规范性、完整性、真实性。随着新修订《中华人民共和国药品管理法》的出台,药物临床试验机构准入管理由资格认定改为了备案管理。2019年11月,国家药品监督管理局会同国家卫生健康委员会出台《药物临床试验机构管理规定》,明确提出对新备案的药物临床试验机构或者增加临床试验专业、地址变更的,应当在60个工作日内开展首次监督检查。为进一步贯彻落实国家京津冀协同发展战略及相关法规政策要求,构建促进药物临床试验监管领域协同发展、高质量发展的标准体系及制度保障,北京市药品监督管理局、天津市药品监督管理局、河北省药品监督管理局协商,决定共同研究制定《京津冀药物临床试验机构备案后首次监督检查标准》(以下简称备案检查标准),进一步规范三地药物临床试验机构备案管理,切实有效实施事中事后监管,形成合力,强化质量管理,服务新药项目研发,促进新药研究成果向生产力转化。
二、起草依据
依据《中华人民共和国药品管理法》《中华人民共和国疫苗管理法》《药品注册管理办法》《药物临床试验机构管理规定》《药物临床试验质量管理规范》等法规、规章及规范性文件,结合京津冀三地实际情况,北京市药品监督管理局会同天津市药品监督管理局、河北省药品监督管理局起草了《京津冀药物临床试验机构备案后首次监督检查标准(征求意见稿)》。
三、主要内容
备案检查标准分为机构、伦理委员会、专业、Ⅰ期临床试验研究室四个部分,包括19个检查环节、66个检查项目。其中关键项目13项(标示为“★”),一般项目53项。
机构部分包括6个环节,分别为资质条件、组织机构与人员、场所与设施设备、质量体系文件管理、质量管理、应急与抢救;伦理部分包括4个环节,分别为伦理委员会备案、组成与人员、场所与设施设备、制度文件与文档管理;专业部分包括4个环节,分别为专业资质、组织机构与人员、专业条件及设施设备、质量体系文件管理;Ⅰ期临床试验研究室部分包括5个环节,分别是资质与条件、组织管理与人员、场所与设施设备、质量体系文件管理、质量管理。
备案检查标准采用表格式设计,设置了检查环节、检查项目、关键项,其中检查项目明确了检查主要内容及应满足的标准要求。根据风险程度将检查项目分为关键项目和一般项目两个等级。关键项目主要涉及机构、伦理、专业的资格资质及急危重病症抢救等方面,其余检查项目为一般项目,体现机构、伦理及专业应具备的相关条件。检查中发现不符合要求的项目统称为“缺陷项目”。其中,关键项目不符合要求者称为“严重缺陷”,其他项目不符合要求者统称为“一般缺陷”。
检查结果按机构、伦理委员会、专业、Ⅰ期临床试验研究室四部分分别评定。各检查部分均未发现严重缺陷,且一般缺陷≤20%,判定为通过首次备案检查。发现严重缺陷,或一般缺陷>20%的,判定为未通过首次备案检查,对发现的问题应立即组织整改。涉及机构或伦理委员会未通过备案检查的,整改期间该机构不得开展新的药物临床试验项目;涉及专业、Ⅰ期临床试验研究室未通过备案检查的,整改期间相关专业、Ⅰ期临床试验研究室不得开展新的药物临床试验项目。整改完毕后向所在地药品监管部门提交整改报告及跟踪检查申请,现场检查符合要求后,方可开展新的药物临床试验。
附件3
京津冀药物临床试验机构日常监督检查标准
(征求意见稿)
总 则
一、为加强京津冀药物临床试验机构监督管理,提升药物临床试验质量管理水平,根据《中华人民共和国药品管理法》《中华人民共和国疫苗管理法》《药品注册管理办法》《药物临床试验质量管理规范》《药物临床试验机构管理规定》《药物临床试验伦理审查工作指导原则》等法律法规及规范性文件,制定本检查标准。
二、本检查标准适用于京津冀行政区域内药物临床试验机构的日常监督检查。
三、检查标准分为机构、伦理委员会、专业三个部分,包括30个检查环节、120个检查项目。其中关键项目15项(标示为“★”,均为必查项),一般项目105项。
四、检查中发现不符合要求的项目统称为“缺陷项目”。其中,关键项目不符合要求者称为“严重缺陷”,一般项目不符合要求者称为“一般缺陷”。
五、检查结果评定
检查结果按机构、伦理委员会、专业三部分分别评定。
(一)各检查部分均未发现严重缺陷,且一般缺陷≤20%,要求机构对发现的问题应立即组织整改,并于10个工作日内将整改情况报告报送所在地药品监管部门,整改期间机构可继续承接药物临床试验。
(二)发现严重缺陷,或一般缺陷>20%的,判定为未通过检查,对发现的问题应立即组织整改。涉及机构或伦理委员会未通过检查的,整改期间该机构不得开展新的药物临床试验项目;涉及专业(包括Ⅰ期临床试验研究室)未通过备案检查的,整改期间相关专业不得开展新的药物临床试验项目。整改完毕后应向所在地药品监管部门提交整改报告及跟踪检查申请,现场检查符合要求后,方可开展新的药物临床试验;涉及违法行为的,依法查处,并向所在地省级卫生健康主管部门通报。
A.药物临床试验组织管理机构检查项目


注:A.药物临床试验组织管理机构检查项目包括8个检查环节、29个检查项目,其中关键项目3项,一般项目26项。
**
B.伦理委员会检查项目
**


注:B.伦理委员会检查项目包括7个检查环节、26个检查项目,其中关键项目3项,一般项目23项。
**
**
C.专业检查项目
**
**
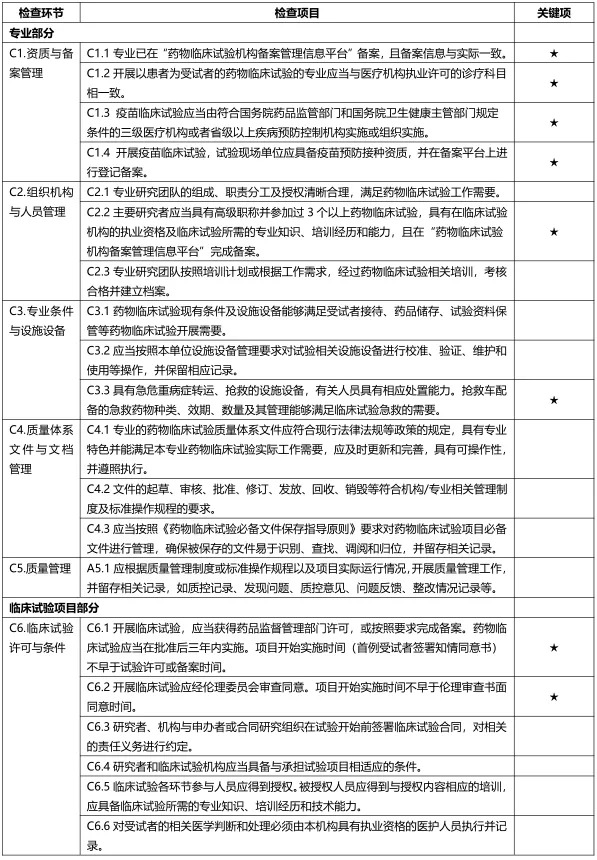



注:C.专业检查项目包括15个检查环节、65个检查项目,其中关键项目9项,一般项目56项。
附件4
《京津冀药物临床试验机构日常监督检查标准(征求意见稿)》起草说明
一、起草背景
截至2021年2月,京津冀地区共有已备案药物临床试验机构近140家,约占全国备案药物临床试验机构总数的13%。针对药物临床试验机构开展科学、有效的日常监督管理,是促进药物临床试验规范实施,试验数据完整、准确,受试者安全及合法权益得到有效保障的重要措施,也是监管部门落实事中事后监管的重要举措。近年来,随着我国药品研发的快速发展和药品审评审批制度改革的深化,我国药品监管法规政策发生了较大变化,国家相继修订了《中华人民共和国药品管理法》《药品注册管理办法》《药物临床试验质量管理规范》,出台了《中华人民共和国疫苗管理法》《药物临床试验机构管理规定》等法律法规及政策文件,对药物临床试验机构准入及运行管理、药物临床试验项目审批管理、药物临床试验质量管理等方面提出了新的规定、新的要求,如药物临床试验机构准入管理由审批改为备案,药物临床试验实施默示许可,生物等效性试验改为备案管理,质量管理规范与国际接轨等。为进一步贯彻落实国家京津冀协同发展战略,构建促进药物临床试验监管领域协同发展、高质量发展的标准体系及制度保障,北京市药品监督管理局、天津市药品监督管理局、河北省药品监督管理局协商,决定共同研究制定《京津冀药物临床试验机构日常监督检查标准》(以下简称日常监督检查标准),以适应新形势下监管工作的需要,进一步规范三地药物临床试验机构日常监督管理,提升三地药物临床试验质量管理水平,服务医药产业高质量发展。
二、起草依据
日常监督检查标准是京津冀三地药品监管部门对药物临床试验机构实施监督管理的指导和依据,也是药物临床试验机构加强内部管理的重要参考。根据《中华人民共和国药品管理法》《中华人民共和国疫苗管理法》《药品注册管理办法》《药物临床试验机构管理规定》《药物临床试验质量管理规范》等法规、规章及规范性文件,参考《北京市药物临床试验机构日常监督检查标准(试行)》《天津市药物临床试验机构监督检查要点》,结合京津冀三地实际,北京市药品监督管理局会同天津市药品监督管理局、河北省药品监督管理局共同研究起草了《京津冀药物临床试验机构日常监督检查标准(征求意见稿)》。日常监督检查标准的制定工作以“依从性、规范性、可操作性”为指导思想,以“过程监管、风险控制”为基本原则,既关注机构备案条件的持续符合性,同时还突出对药物临床试验机构运行及项目实施过程合规性、数据可靠性的动态监管。
三、主要内容
日常监督检查标准分为机构、伦理委员会和专业三个部分,包括30个检查环节、120个检查项目。其中关键项目15项(标示为“★”),一般项目105项。
机构部分包括8个检查环节,分别为备案管理、组织机构与人员、场所与设施设备、质量体系文件及文档管理、试验药品管理、质量管理、应急与抢救、其它;伦理委员会部分包括7个检查环节,分别为伦理委员会备案、组成与人员、场所与设施设备、制度文件与文档管理、伦理审查、安全性信息的处理、其它;专业部分分为专业和临床试验项目两个方面,包括15个检查环节,分别为资质与备案管理、组织机构与人员管理、专业条件与设施设备、质量体系文件与文档管理、质量管理、临床试验许可与条件、伦理审查、知情同意、受试者筛选及方案执行、临床试验数据和文档管理、临床试验数据溯源、试验用药品管理、安全性信息管理、委托研究及其它检查环节。
日常监督检查标准采用表格式设计,设置了检查环节、检查项目、关键项,其中检查项目明确了检查主要内容及应满足的标准要求。根据风险程度将检查项目分为关键项目和一般项目两个等级。关键项目主要涉及机构、伦理、专业的资格资质、急危重病症抢救、数据真实性等方面,其余检查项目为一般项目。检查中发现不符合要求的项目统称为“缺陷项目”。其中,关键项目不符合要求者称为“严重缺陷”,其他项目不符合要求者统称为“一般缺陷”。
检查结果按机构、伦理委员会、专业项目三部分分别评定。各检查部分均未发现严重缺陷,且一般缺陷≤20%,要求机构对发现的问题应立即组织整改,并于检查结束10个工作日内提交整改情况报告,整改期间机构能够继续承接药物临床试验;发现严重缺陷,或一般缺陷>20%的,判定为未通过检查,对发现的问题应立即组织整改,涉及违法行为的,依法查处,并向机构所在地省级卫生健康主管部门通报。涉及机构或伦理委员会未通过检查的,整改期间该机构不得开展新的药物临床试验项目;涉及专业(包括Ⅰ期临床试验研究室)未通过备案检查的,整改期间相关专业不得开展新的药物临床试验项目。整改完毕后向所在地药品监管部门提交整改报告及跟踪检查申请,现场检查符合要求后,方可开展新的药物临床试验。
附件5
征求意见反馈表
征求意见稿名称: